PDE4阻害剤 オテズラ錠 10mg,20mg,30mg (一般名: アプレミラスト錠 )が 2017年3月1日に発売開始となったんやけど知ってる? 製造販売会社は セルジーン株式会社 。国際的にみると,この薬はなんと約 25年ぶり に出る 乾癬 の飲み薬による新薬やねんで!(日本で見れば,ネオーラルが出たのが2000年なので17年ぶり)乾癬の薬といえば,ここ最近はマルホが出した別に大したこともないくせに高いだけの マーデュオックス軟膏 くらいなもんやったのでちょっと興味惹かれるよね!?
そんなわけで,けいしゅけのブログ薬局情報館が勝手に勉強会をしたので報告書として記事にまとめてお届けします☆
- 乾癬ってなんやったっけ?復習
- オテズラ錠より前に出ていた内服の薬って・・・なんだったっけ?思い出そう
- オテズラ錠の作用機序を調べる
- 錠剤の安定性など特徴を調べる
- 服用方法を確認
- 使用上の基本的な注意を確認
- 代表的な副作用はどんなものがあるのか?しっかり知っておく
- 食事によって吸収量が増えたり減ったりしないかチェック
- 肝代謝型?腎排泄型?
- 肝臓・腎臓が悪い人に投与した場合の血中濃度はどうなる?
- 薬価と長期処方解禁がいつかもチェック!
- おまけ:セルジーンって製薬会社・・・聞いたことないんですけど?どんな会社?調べてみた
- まとめ
[/list]
こんな流れで行こうかと思います!!この記事を読めばオテズラ錠についての基礎情報は網羅できると思うで☆
ほな,いくズラ~
オテズラ錠は乾癬の治療薬というけど,乾癬ってどんな病気だった?
まずは基本的なところから。乾癬というのはいまだに原因が特定されていない皮膚疾患の事や。ひとまず言える原因は免疫異常が生じていることによって炎症反応の異常が生じているってこと。症状に関しては人によって様々やけど,代表的な尋常性乾癬(乾癬の90%は尋常性乾癬)では,頭皮や肘,ヒザ,腰,拳などにかゆみを伴う銀白色の鱗屑を伴う紅斑が現れる慢性炎症性角化症やったよね。
詳しい症状から治療法については,乾癬とはどんな病気やろ?原因や治療薬・治療法をまとめたで!にまとめているので参照してほしい。 [/box]
25年ぶりというけれど,オテズラ錠より前に出ていた内服薬って何やっけ?
さらっと言えちゃうで☆って人はこの項目は読み飛ばしてください。
ひとまず復習として書いておきます。今まで出ていた内服薬は3つ。販売開始順に書いていこう。
チガソンカプセル 10mg / 25mg ・・・販売開始1985年
まずはチガソンカプセル。1985年12月の販売開始のお薬や。2017年現在の薬価は 10mgで324.2円, 25mgで827.1円
販売開始から30年以上たってもこの薬価。高い!ジェネリック医薬品も出てない。
乾癬といえばチガソン!ってくらいメジャーで基本的な薬剤やね。ビタミンAの誘導体で角化症治療剤。副作用発現率は70%を超える!
代表的な副作用は口唇炎。唇がガッサガサになるねん。ほかにも皮膚がポロポロ剥がれ落ちる落屑,口内の乾燥,皮膚が薄くなる,などといった副作用が出てしまうのが特徴的やってん。
これは実は仕方がなくて,作用機序としてチガソンカプセルの成分であるエトレチナートが,皮膚をポロポロと落として(落屑させて)から,正常な上皮の再形成になるように働くためやってん。乾癬の部分の皮膚だけならいいんやけど,それ以外の皮膚も同じように落屑してしまうという。作用と副作用が密接に絡んでしまっていたというわけや。
- 催奇形性がある!妊婦または妊娠の可能性のある患者には投与NGや。
- 催奇形性があるので,投与中止後,男性で6か月間,女性は2年間は避妊する必要がある。
- 催奇形性があるので,投与中止後2年間は献血してはいけない。
サンディミュンカプセル 25mg / 50mg ・・・販売開始1991年
次がサンディミュンカプセル。1991年1月の販売開始のお薬や。2017年現在の薬価は 25mgで250.2円, 50mgで442.5円
これに関してはジェネリック医薬品がある。シクロスポリンカプセルが25mgで94.2円~132.4円, 50mgで173.4円~238.6円で存在するため,自己負担額は軽減できる。
ただし,現在はほとんど処方されることはないねん。なぜなら,次に書くネオーラルカプセルがサンディミュンカプセルの改良版で出ているから。
ネオーラルカプセル 25mg / 50mg ・・・販売開始2000年
最後にネオーラルカプセル。2000年5月に日本で販売開始になっている(国際誕生は1993年2月)。
2017年現在の薬価は 25mgで227.5円, 50mgで394.5円。サンディミュンカプセルよりも値段も安い。
特筆すべき点は,サンディミュンカプセルが経口投与時における吸収量が個人差があるため,成分であるシクロスポリンの体の中での濃度をいちいち計測する必要があったということ。また,グレープフルーツとの併用で濃度がアップ。セイヨウオトギリソウとの併用で濃度がダウンするという不安定さが問題だった。
これを,マイクロエマルジョン製法という方法によって成分であるシクロスポリンを個人差なく吸収されやすく改良されたのんが,ネオーラルカプセルってわけや。この製法はまだ特許で守られているので,ネオーラルカプセルはジェネリック医薬品に変更すると血中濃度が変化する可能性があるので基本的には変更するべきものではないねん。もし患者さんの強い希望によってジェネリック医薬品に変更したんであれば,処方医に変更していることをフィードバックしておくことが大事やで!!
ちなみに,サンディミュンとネオーラルの成分であるシクロスポリンは,乾癬に対してどう効くのか?シクロスポリンは免疫抑制剤。つまり,免疫反応を抑えることによって働くわけ。具体的に話すとけっこうややこしいねんけど,免疫T細胞のカルシニューリンの働きを邪魔することによって,体の中に入ってきた敵をやっつけようとするサイトカインという物質が作られるのをブロックするのだ。乾癬はこの免疫反応がやたらと活発になっているとされているので,抑えてあげることで症状が改善するねん。
 けいしゅけ
けいしゅけオテズラ錠よりも前に出ていた内服薬は以上の3つや。実質的には2つと言っていいけれど。これで,ひとまず復習終わり!
オテズラ錠 ( アプレミラスト )の作用機序, PDE4阻害 を解説します
尋常性乾癬の皮膚組織では何が起こっているのか?がわからないと,オテズラ錠の作用機序は理解が難しい。
正常細胞と比べて尋常性乾癬の皮膚細胞は何がおかしいのか?これは様々な考察があるねんけど,
今のところ考えられているのは免疫細胞から炎症性ケミカルメディエーターである,
- TNF-α(腫瘍壊死因子-α)
- IL-17(インターロイキン-17)
- IL-23(インターロイキン-23)
っちゅうもんが過剰に放出されて皮膚の表面での炎症が亢進した結果,角化を伴う表皮の異常増殖が発生しているのであーる!
っていうものがあるのよ。
最新の研究で分かった新たな原因が, PDE4 の過剰発現による免疫細胞の異常
さっき書いた因子以外で乾癬の原因として示唆されている因子の1つに挙げられているものこそ, PDE4( Phospho Di Esterase 4-ホスホジエステラーゼ4 )の過剰発現ってわけや。
PDE4は,免疫細胞内で cAMP( cyclic Adenosine Mono Phosphate )を不活性型の AMP(Adenosine Mono Phosphate)に分解する酵素で,免疫細胞の中でのシグナル伝達を調節しているねん。細胞の中でcAMP濃度が低くなると人の体の中では,炎症性ケミカルメディエーターの分泌を促進させてしまう。これによって表皮細胞の過剰増殖と角化異常を引き起こしてしまうというのが尋常性乾癬の新たなメカニズムとして考えられているものや。



ややこしいからまとめよう。
- 人の免疫細胞の中のcAMP濃度が下がると炎症性ケミカルメディエーター分泌が促進されるスイッチがオンになる
- そのcAMPの濃度が下がる原因は,これを分解してAMPにしちゃう PDE4 という酵素
- これが尋常性乾癬患者さんの免疫細胞内では異常増殖している!
ほんでもって,その結果が,表皮細胞の過剰増殖と角化異常ってわけね。
よっしゃ,ここまではなんとなくわかった。ほんじゃオテズラの作用機序をまとめるズラ!!
オテズラ は低分子の PDE4阻害剤 。これによってcAMP濃度の低下を防ぐのが作用機序じゃ!
オテズラの作用機序をまとめていこう。
オテズラはさっき説明したPDE4という酵素にくっついて,PDE4がcAMPをAMPに分解する働きを邪魔するねん。結果として,免疫細胞内のcAMPの濃度が上昇するから,炎症性・抗炎症性のケミカルメディエーターの分泌が調節されるってわけ。
尋常性乾癬患者の場合ならケミカルメディエーターの分泌が促進されていたわけやから,オテズラによってこの分泌がちょうどいい程度まで抑制されるってわけや。



この作用機序は従来の乾癬治療薬には一切なかったものやねん。なので非常に新しく,画期的なわけ。ちなみに,臨床試験においては尋常性乾癬患者の表皮肥厚の減少・炎症関連遺伝子の発現低下・炎症性細胞浸潤の減少を認めたんやってさ。せやけど,作用機序については今もなお研究を進めている最中。まだまだ乾癬の原因も,これに対してなぜ・どのようにこの薬が効くのかは完全解明に至ってないんやね。
オテズラ錠 ( アプレミラスト )は脱ヒート・1包化できるのか?錠剤の安定性をチェック!
さてさて,ここまでわかれば,あとは調剤するにあたって,この薬が取り扱いやすいかどうかが気になってくる。
いわゆる成分や製剤の安定性ってやつ。これをまとめていくで。先に行っておくと,けっこうええ感じやで!
成分の安定性について
まずは成分について。 アプレミラスト は白色から痰黄色の粉末で,相対湿度(relative humidity,以下略記: RH)0~95%で 吸湿性は認められなかった 。
- 長期保存試験:保存条件⇒25℃/60%RH 保存形態⇒ポリエチレンバッグ+高密度ポリエチレンドラム 保存期間⇒36カ月 結果⇒異状なし
- 加速試験:保存条件⇒40℃/75%RH 保存形態⇒ポリエチレンバッグ+高密度ポリエチレンドラム 保存期間⇒6カ月 結果⇒異状なし
- 過酷試験(光):保存条件⇒昼光色蛍光灯 近紫外蛍光ランプ 保存期間⇒総照度⇒240万lux・hr 総近紫外線放射エネルギー⇒420w・hr/㎡ 結果⇒異状なし
以上からわかるのは,ひとまず,成分である アプレミラスト については,メッチャ安定しているってことやね。
製剤の安定性について
- 長期保存試験:保存条件⇒30℃/65%RH 保存形態⇒PTP包装 保存期間⇒36カ月 結果⇒異状なし
- 加速試験:保存条件⇒40℃/75%RH 保存形態⇒PTP包装 保存期間⇒6カ月 結果⇒異状なし
- 光安定性:保存条件⇒白色蛍光灯 近紫外蛍光ランプ 開放条件⇒総照度⇒240万lux・hr 総近紫外線放射エネルギー⇒420w・hr/㎡ 結果⇒異状なし
ここでもやはり安定している。



結論!メッチャ安定しているから1包化は問題なしと考えられる!半錠にすることと,粉砕調剤については情報がないので今のところ不明や。ひとまずやらない方がいいと思う!
オテズラ錠 の 服用方法 について。服用開始の用量が特殊なので絶対チェックしておいて!
オテズラ錠は飲み始めは低用量からスタートして漸増していくのが特徴やから絶対に覚えておこう。
理由は,副作用低減のため。いきなり維持量の1回30mgにしてしまうと,悪心・嘔吐,下痢の発現率が高いことが示されているため。
服用開始時の用法・用量について ~ スターターパック があるので安心やけどね~
- 服用開始1日目 朝に10mgを服用 初日は1日1回のみの服用
- 服用開始2日目 朝に10mgを服用 夕に10mgを服用
- 服用開始3日目 朝に10mgを服用 夕に20mgを服用(3日目の夕食後から増量になる)
- 服用開始4日目 朝に20mgを服用 夕に20mgを服用
- 服用開始5日目 朝に20mgを服用 夕に30mgを服用(5日目の夕食後から再び増量する。維持量に到達)
- 服用開始6日目 朝に30mgを服用 夕に30mgを服用
- 服用開始7日目 朝に30mgを服用 夕に30mgを服用
[/list]
以上のようにして,徐々に服用量が増えていくのが オテズラ錠 の飲み方でまず押さえておかないといけないところ。
ちなみに,この7日分がスターターパックとして販売されているので,発注しておけば,台紙にセットされているので調剤はカンタン。
大変なのは事務さんの入力やと思う。この記事を読んだら,ひとまず入力方法を各薬局で確認すべしやで!
重度の腎機能障害患者さんへの投与方法
後述するけれど,このオテズラ,重度の腎機能患者さんにおいては血中濃度が上昇することがわかっているので用量調節が必要になる。
用量の調節は維持量を血中濃度の測定から割り出されるので,確認のもと,医師の指示に従えばいい。
薬剤師が知っておきたいのは服用開始の際の用法や!
もしも1日1回30mgを投与となった場合,投与開始時は以下の通りに調剤し,服用させよう
- 服用開始1日目 朝に10mgを服用 初日は1日1回のみの服用
- 服用開始2日目 朝に10mgを服用
- 服用開始3日目 朝に10mgを服用
- 服用開始4日目 朝に20mgを服用
- 服用開始5日目 朝に20mgを服用
- 服用開始6日目 朝に30mgを服用
- 服用開始7日目 朝に30mgを服用
[/list]
こんな感じ。
つまり,スターターパックの朝の分だけ飲んでもらうねん!
勉強不足でした!追記します!!
高度腎機能低下患者さんへの投与方法~実践編~
投与する場合は,スターターパックの1日目から1日1回服用。パックの1日目の左側の朝の分から,左⇒右⇒翌日の左⇒右と1日1回で服用していく。
1日目 10mg
2日目 休薬
3~5日目 10mg
6~9日目 20mg
10日目以降 30mg
で継続服用していく。これによってスターターパックに入っている薬は1錠たりとも無駄になりませんので,服薬指導の際にこの情報をお使いくださいませ。
Twitterでフォローさせていただいている方から情報提供をいただきました。
ありがとうございます!感謝いたします。
オテズラ錠 ( アプレミラスト )の 使用上の注意を確認しよう
いくつか重要な注意点があるのでしっかりとまとめていこうと思う。
妊婦または妊娠している可能性のある女性に禁忌 理由は2つの動物実験結果から
①:マウスで臨床用量の2.3倍に相当する要領で早期吸収胚数および着床後胚損失率の増加,胎児体重の減少,骨化遅延が認められた。
②:サルで臨床用量の2.1倍に相当する用量で流産が認められている。
これら2つの動物実験の結果から,ヒトにおいて胚胎児毒性を引き起こす可能性が否定できないから。
よって,妊娠可能な女性に対しては投与前に問診などによって妊娠していないことを確認し,オテズラが胚や胎児に対して毒性のリスクがあることを説明したうえで投与を開始し,投与期間中は適切な避妊を行うよう指導すること。
これは医師だけが確認していればいいもんじゃない。ちゃんと投薬する際に女性に処方されていれば,胎児への毒性リスクがあることを医師から聞いているのか?今は妊娠していないか?をちゃんと確認しよう。
避妊することを説明するような指導箋があれば必ず添付してお渡ししよう!
オテズラ錠 ( アプレミラスト )の 副作用 について
それでは副作用についてまとめていくで。
やっぱり服薬指導においても重要な知識なので,しっかりと知っておこうね。
国内臨床試験における 副作用 発現状況
対象例数:241例
副作用発現例数:71例
副作用発現率:29.5%
けっこう副作用が出ている印象やね。
具体的な 副作用の内容 とは?⇒ほとんどが胃腸症状
発現した副作用で,主なものとしては以下の通り。
- 下痢11例(4.6%)
- 腹部不快感9例(3.7%)
- 鼻咽頭炎8例(3.3%)
- 軟便6例(2.5%)
- 乾癬5例(2.1%)
- 悪心4例(1.7%)
[/list]
以上が承認時の副作用報告の実態や。
ほとんどが胃腸症状であることがわかる。海外での臨床試験における副作用報告でもこの傾向は同じやったらしい。加えるとすれば,
頭痛(5.5%),緊張性頭痛(2.7%),上気道感染(2.7%)という報告が多かったと結果が出ている。
服薬指導時にはこれらが起こる可能性を説明するべきだろうね。
オテズラ錠 ( アプレミラスト )の 吸収量 における食事の影響ついて
ココからはADME,吸収から排泄までの情報をまとめていく。といっても重視したのは吸収と代謝。
まずは吸収や。食事の影響を受けるかどうかで,食前服用なのか食後服用なのかが変わってくるからね。
外国人のデータ:高脂肪食の摂取とオテズラの吸収量について,結果は影響なし
健康成人46例にアブレミラスト30mgを空腹時投与および高脂肪食(タンパク質,炭水化物および脂肪からそれぞれ約150,250および500~600キロカロリーを摂取)の開始30分後に投与した時のtmax(中央値)は,空腹時投与では2.5時間で食後投与では3.0時間だった。
ちなみにアプレミラストのAUCおよびCmaxはほぼ同等で,いずれも幾何平均値比%の 90%CIが80~125%の範囲に含まれていた。
この結果から,アプレミラストの吸収および暴露に対する食事の影響は認められなかった。
ちなみに,アプレミラストの消化管からの吸収率は84.4%と示唆されている(外国人データより)



つまり,オテズラ錠は食事に関係なく服用していいって意味ずら!食後に飲んでもいいし,理由があって食事がとれないときでもそのまま飲んだかて,効果に問題はないよ!って患者さんに説明してあげたらええわけや。
肝代謝型 もしくは 腎排泄型 オテズラ錠はどっちかキッチリ確認しよう
次は超重要な,代謝について。
代謝部位:【in vitro:試験管内】アブレミラストは,ヒト肝ミクロソームおよび幹細胞により広範に代謝された。
代謝経路:【外国人データより】アプレミラストはチトクロムP450酸化代謝に続くグルクロン酸抱合及びCYP以外の加水分解により代謝され,血漿および尿中のO-脱メチルおよび脱エチル代謝物は,主としてグルクロン酸抱合体として存在していた。



カンタンに言うと,肝代謝型やっちゅう事やね。
2017.5.13 追記 質問があったのでさらに勉強してみました!
アプレミラストの代謝・排泄について
代謝
(1) 代謝部位及び代謝経路
1) 代謝部位 <in vitro>46) アプレミラストは,ヒト肝ミクロソーム及び肝細胞により広範に代謝された。
2) 代謝経路 <外国人のデータ>8) 健康成人男性 6 例に,[ 14C]-アプレミラスト懸濁液 20mg を単回経口投与したとき,
血漿中総放射能の AUC に占めるアプレミラスト(未変化体)の割合は 45%で,
次いで O-脱メチル化アプレミラストのグルクロ ン酸抱合体である不活性代謝物 M12 が 39%認められた。アプレミラストは広範に代謝され,血漿及び排泄物で 23 種類の代謝物が同定された。
アプレミラストはチトクロム P450(CYP)酸化代謝に続くグルクロ ン酸抱合及び CYP 以外の加水分解により代謝され,血漿及び尿中の O-脱メチル及び脱エチル代謝物 は,主としてグルクロン酸抱合体として存在していた。
(4) 代謝物の活性の有無及び比率 46)
アプレミラストの代謝物(M1/M2,M3,M5,M7,M12,M14,M16,M17)の PDE4 阻害及び TNF-α 産生阻害 作用を評価した。
評価した代謝物の中で,M7 及び M17 が in vitro で PDE4 活性及び TNF-α 産生に対し阻 害作用を示したが,これらの薬理作用はアプレミラストよりも弱く,血漿中アプレミラスト濃度に対する割合も 1%未満と極めて少量であることから,代謝物 M7 及び M17 の薬力学的作用に対する明らかな寄与はほとん どないと考えられた。
排泄
(1) 排泄部位及び経路
主に尿中又は糞中に代謝物として排泄される。
(2) 排泄率
<外国人のデータ>8) 健康成人男性 6 例に,[ 14C]-アプレミラスト懸濁液 20mg を単回経口投与したとき,
未変化体の排泄率は尿中 では投与量の 3%未満,糞中では投与量の約4%であった。
薬理学的に不活性な O-脱メチルアプレミラストの グルクロン酸抱合体(M12)が主要な血漿中代謝物であり,
その尿中排泄率は総投与量の約 34%であった。
引用元:オテズラ錠 インタビューフォームより
そう,これを見る限りは殆どが肝臓で代謝されるとある。だからこそ,肝代謝型と読んだ。
しかし,排泄となると,代謝物として尿中及び糞中に排泄されると書いてある。
- 未変化体の排泄率は尿中 では投与量の 3%未満
- 薬理学的に不活性な O-脱メチルアプレミラストの グルクロン酸抱合体(M12)が主要な血漿中代謝物であり,その尿中排泄率は総投与量の約 34%であった。
これなのに,腎機能低下例での血中濃度上昇があるので,用量調整が必要になる本剤。
どういうこっちゃ?
これをどう解釈したらええんやろか?
頭をひねる。 ・・・あ!
思い出したのが,日経DIの山本雄一郎先生の「薬局にソクラテスがやってきた」の過去記事や。
肝臓で代謝や抱合を受ける薬剤について。
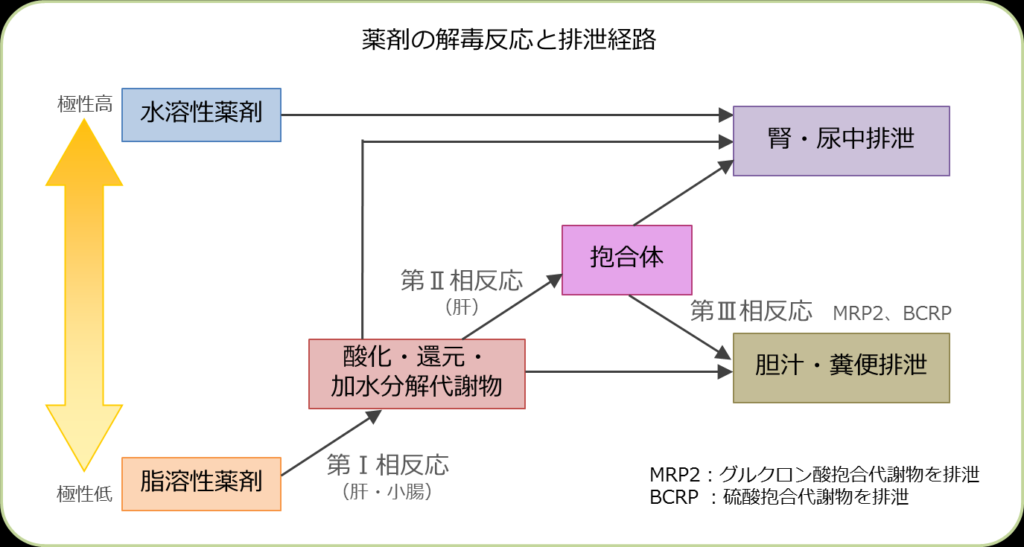
これらは概して脂溶性が高い。脂溶性薬剤は腎臓で糸球体濾過されても,近位尿細管の刷子縁膜において速やかに再吸収されてしまうため,腎・尿中から排泄されることはない。
ゆえに代謝や抱合を受けるわけだ。これらは極性化反応,つまり極性を高めることで胆汁排泄を促し,腎臓では再吸収を受けないようにしている。
もちろん例外もある。fuの高いアマンタジン塩酸塩(シンメトレル他)やプラミペキソール塩酸塩(ビ・シフロール,ミラペックス他),ミルナシプラン塩酸塩(トレドミン)は,実は脂溶性が高い。これらは尿細管分泌によって腎排泄されている。アマンタジンとプラミペキソールはOCT(有機カチオントランスポーター)の基質であり,ミルナシプランについてはその輸送系は明らかになっていない。
そうやって肝臓で代謝を受けた後の,活性を持たない代謝物や抱合体は,胆汁もしくは尿中から排泄される。
その場合,当然ながら,尿中に排泄されるからといって,腎機能に応じた減量をする必要はない。
これらの薬剤は,その消失自体が肝臓の代謝によるために,“肝消失型薬剤”と呼ぶのが正しいのだ。
出典:薬局にソクラテスがやってきた 「肝代謝型,肝排泄型,肝消失型の違いは?」より
この出典を参考にしても,やはりオテズラ錠は「肝消失型」の薬剤であろうと考えられる。
ではなぜ,肝機能ではなく,腎機能が低下した例で血中濃度が上がってしまうのだろう??



アカン・・・今の僕のレベルではこれはわからない。
セルジーン社に問い合わせてみて,答えが分かった時にさらに追記をしようと思います!
[/box]
オテズラ錠 ,肝臓・腎臓が悪い人に投与した場合の血中濃度はどうなる?
血中濃度が上がってしまうケースがあるので,肝機能低下例に投与した時の数値と腎機能低下例への投与の際の血中濃度の数値が健康成人に投与した場合と,どう変わるか知っておこう。
肝機能低下例に投与した場合
【外国人データ】
中等度肝機能障害患者(Child-Pugh 7-9)のAUC∞およびCmaxは,健康成人に比較してそれぞれ5.4%および15.9%低く,
重度肝機能障害患者(Child-Pugh 10-13))のAUC∞およびCmaxは,健康成人に比較してそれぞれ1.6%および34.9%低かったが,
健康成人との幾何平均値比%の 90%CIは100%を含んでおり,顕著な差ではないことが示された。



つまり,肝機能に応じた用量調節は基本的には考えずに投与ができるという事が分かるね。
腎機能低下例に投与した場合
【外国人データ】
軽度および中程度の腎機能障害患者各8例にア@ウレミラスト30mgを単回経口投与した時に,
軽度腎機能障害患者と健康成人との薬物動態に臨床的に意義のある差は認められなかった。
中程度腎機能低下患者と健康成人との薬物動態に対する比較ではAUC∞の幾何平均値が約22%高く,Cmaxの幾何平均値は約13%低くなったが,統計的に 有意差 は認められなかった。
ただし
重度腎機能障害患者8例にアプレミラスト30mgを単回経口投与したとき, 健康成人と比較してAUC∞が約88.5%,Cmaxは41.6%増加した。
[aside type=”normal”] 重度腎機能低下患者に対する用量調節が必要!
血中濃度の上昇の可能性が上記データより示されたため,本剤を30mg1日1回投与するなどの減量を考慮し,慎重投与とする。
ちなみに,1日1回30mgを投与する場合の投与開始時の用量としては,スターターパックの朝の用量のみ投与する!(戦術の通り) [/box]



重度腎機能低下患者さんに気を付けろ!ってことやな。ちなみに,重度腎機能低下っていうのは,eGFR<30やで!
オテズラ錠 ( アプレミラスト )の 薬価 と 長期処方解禁がいつか? もチェック!
薬価について
- オテズラ錠 10mg ・・・324.2円 / 1錠
- オテズラ錠 20mg ・・・648.4円 / 1錠
- オテズラ錠 30mg ・・・972.6円 / 1錠
維持量は1日2回,1回30mgなので,1日薬価は1945.2円 となり,
3割負担患者で583.56円 / 日 ⇒ 17506.8円 / 30日
1割負担患者でも194.52円 / 日 ⇒ 5835.6円 / 30日 となる。
オテズラ錠の長期処方解禁はいつから?
長期処方解禁は,2018年3月から
おまけ:セルジーンって会社は何者?
いやぁ,セルジーンとオテズラの関係って,スピッツとロビンソンの関係に似ているよなぁ?
どっちが会社名でどっちが商品名かわからへんねん。
ってか,セルジーンて何?
気になったのでおまけで調べてみた。
セルジーン:アメリカの会社。1986年にCelenaseより独立した会社。世界的なバイオ医薬品企業としての基盤を築いてきているらしい。
ちなみに今回オテズラ錠を出すのはその日本法人である,セルジーン株式会社。
設立は2005年12月26日。
まだまだ若い会社やね。
うーん,ギリアド社と同じ匂いを感じるわ。
まぁ,オテズラは1錠で何万円もする薬ではないし,バラ錠包装でもないからね。その辺はギリアドより丁寧。
オテズラ錠の包装について
- オテズラ錠スターターパック:27錠【(10mg×4錠,20mg×4錠,30mg×19錠)×1パック】
- オテズラ錠30mg:56錠(14錠PTPシート×4シート)
となっている。
つまり,10mgと20mgはスターターパックにしか入っていないってこっちゃね。
オテズラ錠についての まとめ
長々と書いてきました。乾癬治療薬オテズラ錠(アプレミラスト)。最後にざっくりとした製品情報を羅列して終わります
- 規制区分:劇薬,処方箋医薬品
- 有効期間または使用期限:3年
- 貯法・保存条件:室温保存
- 取り扱い上の注意点:服用時,錠剤をかみ砕いたり,割ったりしないこと(あ!ここで半錠にするなって書いてた!)
- 調剤時の留意点:該当しない・・・(どういうことやねん。)
そのほかについては記事の中でまとめましたのでそちらを参照ください。



今回の記事はいかがでしたか? アナタのお役に立てていれば幸いです! もし良ければコメント欄から記事を読んだ感想や,ご意見,ご質問など寄せて下さい☆待ってます!!











記事の感想など,ひとこと頂けますか?
コメント一覧 (13件)
記事を読ませていただきました。大変勉強になります。
1つ疑問です。未変化体アプレミラストの回収率は、尿中及び糞便中で、それぞれおよそ3%及び4%であった、ということでほとんど加水分解・抱合などで不活性化されているようですが、なぜ肝機能が低下している患者さんではなく腎機能が低下している患者さんのAUCなりCmaxが増加するのでしょうか。
よろしくお願い致します。
しょうへい 様
コメントありがとうございます!
この点については僕も同様に非常に大きな疑問を持っています。
現在、トランスポーターのせいか?など色々と考えをはせています。
セルジーン社にも問い合わせもしておりますが、回答を得るには至っておりません。
この薬の体内動態についての不明点の部分でもあるのかもしれないですね。
もし回答できるような情報が得られた際には記事に掲載しようと思いますので、よろしくお願いいたします!
はじめまして。
彼氏が重度の乾癬にかかっていて、最近主治医さんから新薬が出たけどどうしますかと言われてきました。
おそらくこの薬なのでしょうが、一ヶ月2万円近くかかるので躊躇しているようです。
何か情報がないかと思って検索したらこちらにヒットしました。
わかりやすい文章だし、ほどほどに素人にはわからない専門的内容も盛り込まれていてとても勉強になりました(感謝)。
お酒が好きな人なので、特に夜にきちんと服用できるのか、またアルコールの影響はないのかも心配しています。「飲み合わせ」とは違うでしょうが、そのあたりの情報があるとうれしいです。
たま 様
オテズラ錠とアルコールの相互作用についてなのですが、調べる限りでは今のところ飲み合わせに問題があるというデータはありません。
お酒に関しては多く飲み過ぎになられぬよう御自愛くださればなぁと思います。
食事に関しても特に薬の効果に影響を与えることはないので、もし飲むとなれば経済的な点が最も気になるところかもしれませんね。
あとは負担額に関する点がネックになると思います。
http://www.kansennet.jp/about_care/kougaku/
もし知っていらしたら余計なお世話なのですが、参考になるかもしれません。高額療養費制度についてです。
回答ありがとうございます。
先日タレントの方が乾癬についてカミングアウトをされて多少は病気に対する世間の理解も深まったかなと勇気づけられてもいます。
高額療養費制度についてはぼんやりとしか知らなかったので、これから勉強します!
ありがとうございました。
はじめまして。
先日の診察の時、主治医から「新薬が出ましたよ」との話があり、気になっていました。薬の作用と代謝メカニズムは大変参考になりました。私は今のところ症状が出ているのは腕だけなので、薬の費用を考えると、まだいいかな、と思っています。乾癬患者は増えているそうなので、薬価が下がって使いやすくなればいいと思います。
こんにちは。たまたまヒットした記事でしたが、大変興味深く読ませて頂きました。
私は、このお薬の治験経験者です。
病歴は長く、もうかれこれ20年以上になります。それまでは、何を試してもダメでした。
症状は両足ひざ下が錦鯉状態。肘も真っ赤、背中やお尻にも点々とある状態。
でも、薬を飲み始めて約1週間程度で、かゆみがほぼ無くなり、とても楽になりました。
(おそらく初めからプラセボではなく当りの薬だったと思われます)
その後もみるみるうちに症状が改善して、約1年後の治験終了時には99%完治していました。
(わずかに跡が残っている程度です。かゆみ、赤味も無し)
なんと劇的な効果だと感動しましたね。副作用らしい副作用も私は無かったです。
「薬を止めたら、元の状態に戻ってしまうはずです。」との説明を受けてましたが、その後2年近く経ってますが、5㎜程度の赤味が全身でも5個程度、かゆみはほぼ無しの状態を維持しています。
(ドボネックスは使っています。1本が半年以上持つ程度の使用頻度です)
アプレミラストの日本での認可を心待ちにしておりましたが、現在飲むには症状が軽すぎます。(笑)
たまたま私との相性が非常に良いお薬だったという事も考えられますが、現在乾癬に苦しまれている方々への希望の光になればと思い、私の経験をコメントさせて頂きました。
ぴーころ 様
コメントありがとうございます☆
実際に飲んでみて、改善したよ!という声があるというのは乾癬患者さんにとってすごく勇気づけられる体験談やと思います!
本当にありがたいコメントを頂戴しました。ありがとうございます!
はじめまして。
今日、皮膚科に行ったら「新しい治療薬が出ました。」とパンフレットをもらいました。
乾癬歴は40年程。いろいろな治療をしてきましたが、どれも効果が無く かと言って注射や点滴の治療はあまりにも高額過ぎてあきらめていました。
先生は 積極的ではなかったので、帰って検索していたところ こちらにたどり着きました。
一番気になるけど 情報サイトには明記されていない 月の負担額まで!ありがとうございます。
現在、更年期症状でホルモン補充療法中ですが、この薬併用しても問題ないか情報ありませんでしょうか。
ちゃお 様
コメントありがとうございます。
オテズラ錠のインタビューフォームという詳しい説明書のようなものがあるのですが、
そちらを調べた限りではホルモン補充療法との併用も問題としては挙げられておりませんよ☆
はじめまして。
私は、32年前に突然乾せんを発症しました。
色々薬も試しましたが、
一進一退…………最終的には、身体の湿疹は部分的に縮小?されてきたものの、
頭皮の湿疹が頭全体に広がり、フケ状のものが大量に肩や背中に落ちてくるので、黒い服を着ることを諦めていた毎日でした。
そんな中、
今年の3月にかかりつけ医から、オテズラの事を紹介されて、速攻飛びつきました✨✨
これまで、便秘に悩んでいた私だったのですが、嬉しい誤算は、毎日のビックリするくらいのお通じ
これは、今でも気持ちの良いくらいに続いています。
最初は、
ムカムカ【吐き気まではいかない】とか、頭痛、喉の違和感、咳が続いたのですが、もともとアレルギー性鼻炎と喘息気味もあるので、アレルギーの担当医からも、皮膚科の担当医からも確認してみましたが、関連性は指摘されなかったので、オテズラとの因果関係はわかりません。
今は、そのような症状もなく、
塗り薬も使うこともなく、
あれだけ悩みの種だった頭皮も、1ヶ月しないうちに、黒い服を気にせずに着られるまでになり、今では全く無い状態です。
私が通っている病院では、私を含めて三人だそうですが、私が一番効果があるというか、『合ってるんですね。』…………と、主治医からも言われています。
ただ、
2週間分しかお薬がでないことと、薬価が高いことが難点ですが、これまで悩んでいたことを考えると、続けたいお薬です。
そんな中、始める前も検索していましたが、こちらの【オテズラ情報】は、私が知りたかった情報が沢山載せられていて、本当に有難いです✨✨
ネットで調べると、色々な情報が飛び交っているので、どちらを信じて良いのか困る時がありますが、とても納得のいく、そして為になる内容で勉強になりました。
今後も、新しい情報がありましたら、どうぞこれからも宜しくお願いいたします。
ゆかママ 様
コメントありがとうございます!
すごいすごいっ!お薬が効いて、外に出るのに好きな洋服を色味を気にすることなく来て出かけられるって本当に素晴らしいことですよね☆
読んでいてすっごく嬉しくなりました!
そして、情報提供としてゆかママ様にとってお役に立てたことを光栄に思います!
今後もお役に立てる記事を書いていこうと思いますのでよろしくお願い致します
8歳で尋常性乾癬を発症、乾癬歴40年で関節性症乾癬になりました。医師からオテズラかバイオでの治療をしてみませんかと言われ、ある程度の知識はあったものの、ネットで検索しこちらで勉強させていただきました。軽快な文章でとてもよかった(笑)
副作用に’乾癬’とあり、悪化する可能性もゼロではないのだなぁと不安もありますが、チャレンジしたいと思います。